上海交大瞿旭东团队发现首例双氧杂Diels-Alder酶
【SynBioCon】获悉,近日,上海交通大学张江高等研究院、生命科学技术学院瞿旭东团队联合澳大利亚昆士兰大学Mehdi Mobli团队、上海交通大学生命科学技术学院赵一雷团队及孔旭东团队,在《Nature Chemistry》发表题为“An enzymatic dual-oxa Diels-Alder reaction constructs the oxygen-bridged tricyclic acetal unit of (-)-anthrabenzoxocinone”的研究论文,首次揭示了一种新型双氧杂Diels-Alder (HDA)酶的催化机制,该酶负责II型聚酮天然产物(-)-anthrabenzoxocinone((-)ABX)中手性三环缩酮氧桥结构单元的形成。
生命科学技术学院博士后闫晓丽与昆士兰大学贾新颖博士为论文共同第一作者,瞿旭东教授、Mehdi Mobli教授以及赵一雷教授为论文共同通讯作者;孔旭东长聘教轨副教授,籍顺佳和张梦洁等同学为共同作者。
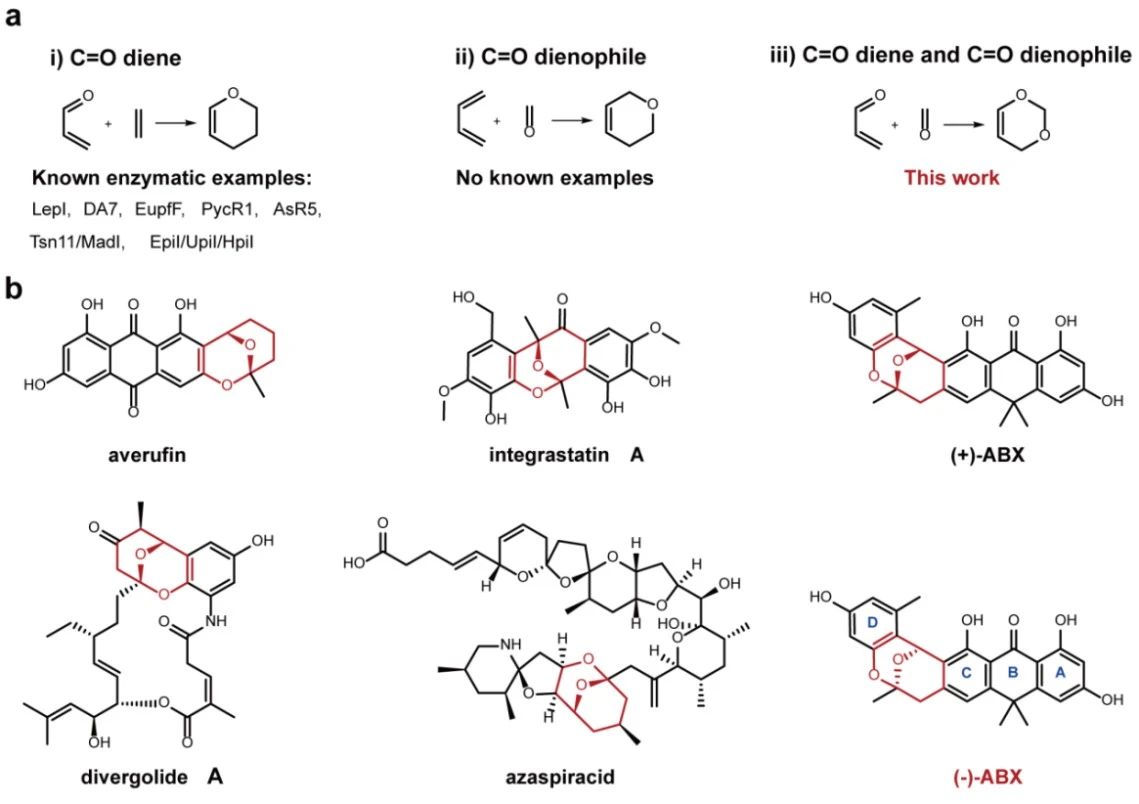
杂Diels-Alder反应(HDA)是构建六元杂环化合物最高效的方法之一,在药物化学、材料科学及天然产物合成中具有广泛应用。其中,氧杂HDA反应(即二烯或亲二烯中含氧原子)是最常见的类型,能够高效构建含氧杂环骨架。然而,尽管自然界已发现多种催化单一氧杂HDA反应的酶(如LepI、EupfF、Tsn11等),双氧杂DA反应(即同时涉及两个氧原子的[4+2]环加成)却从未被报道,其催化机制与酶学基础完全未知。
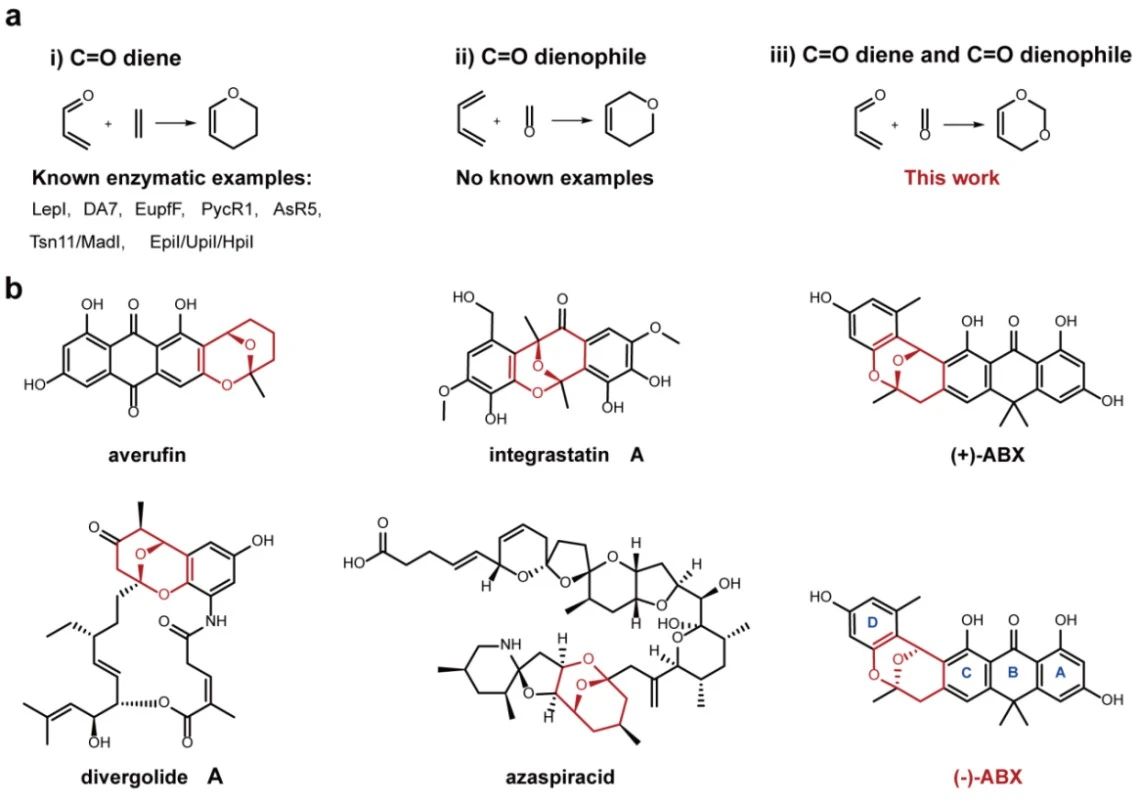 瞿旭东课题组长期致力于分子骨架的生物合成研究。前期工作已阐明(-)ABX中的四环芳香母核的形成机制(Proc Natl Acad Sci USA 2024, 121, e2321722121),但其中三环缩酮氧桥这一关键结构单元的生物合成机制仍悬而未决。值得注意的是,这类三环缩酮氧桥结构广泛存在于多种具有重要生物活性的天然产物中(图1b),其独特的刚性构象对分子的药理活性具有决定性影响。因此,解析其生物合成机制对天然产物化学与创新药物研发具有重要意义。
瞿旭东课题组长期致力于分子骨架的生物合成研究。前期工作已阐明(-)ABX中的四环芳香母核的形成机制(Proc Natl Acad Sci USA 2024, 121, e2321722121),但其中三环缩酮氧桥这一关键结构单元的生物合成机制仍悬而未决。值得注意的是,这类三环缩酮氧桥结构广泛存在于多种具有重要生物活性的天然产物中(图1b),其独特的刚性构象对分子的药理活性具有决定性影响。因此,解析其生物合成机制对天然产物化学与创新药物研发具有重要意义。
本项目中,联合研究团队通过系统的体内外实验,首次发现VOC超家族蛋白Abx(-)F是一种具有双重催化功能的DA酶:其首先催化了脱水反应,将化合物2转化成具有特定轴手性的邻醌亚甲基(o-QM)中间体(Z, Ra)-3;其次,立体选择性地催化(Z, Ra)-3发生分子内双氧杂DA反应,精确构建手性三环缩酮氧桥结构。研究团队进一步综合运用X射线晶体衍射、核磁共振(成功解析Abx(-)F及其与底物的复合物结构)及计算化学等方法,揭示了"脱水-配位协同HDA"这一全新催化机制(图2),为理解该类复杂结构的生物合成提供了范式转变。
本研究的科学意义体现在多个维度:
(1)酶学新发现:鉴定出首例双氧杂HDA酶,不仅填补了多杂原子Diels-Alder酶研究的空白,更预示着自然界可能存在一个全新的多杂原子HDA酶家族,极大拓展了酶促HDA反应的认知维度;
(2)天然产物合成突破:为理解广泛存在的缩酮氧桥结构提供了首个酶学模板,解决了该领域长期悬而未决的关键科学问题;
(3)聚酮化学新认知:(-)-ABX中的缩酮氧桥结构代表着近万种II型聚酮化合物中发现的第9个骨架类型,也是继课题组近期发现的第1个手性骨架(J Am Chem Soc 2025, 147, 5596-5601)之后的第2个手性骨架,为复杂芳香聚酮的理性设计奠定了重要基础。
该研究不仅深化了对HDA反应化学多样性的理解,更为天然产物的定向生物合成和酶工程提供了创新工具,相关技术有望应用于高价值含氧杂环化合物的绿色制造。
本论文研究获得了国家重点研发计划、国家自然科学基金、上海市学术/技术研究领军人才计划等项目的资助。
参考信息:
公开信息
说明:
本平台发布仅为了传达一种不同观点,不代表对该观点赞同或支持。如果有任何问题,请联系 15356747796




